Produtos
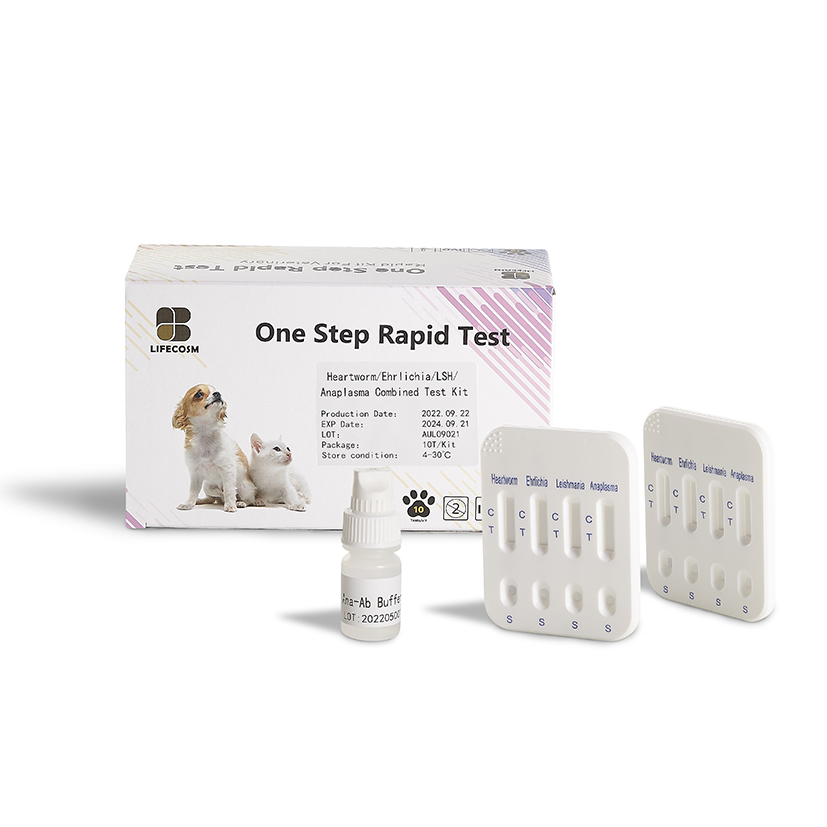
Kit de teste Lifecosm CHW Ag/Anaplasma Ab/E. canis Ab/LSH Ab
Kit de teste CHW Ag/Anaplasma Ab/E. canis Ab/LSH Ab Kit de teste para dirofilariose canina Ag/Anaplasma Ab/Ehrlichia canis Ab/Leishmania Ab
| Número de catálogo | RC-CF31 |
| Resumo | Detecção de antígenos de Dirofilaria immitis canina, anticorpos de Anaplasma, anticorpos de E. canis e anticorpos de LSH em 10 minutos |
| Princípio | Ensaio imunocromatográfico de uma etapa |
| Alvos de detecção | CHW Ag: Antígenos de Dirofilaria immitis Anapalsma Ab: Anticorpos de AnaplasmaE. canis Ab: anticorpos contra E. canis LSH Ab: L. chagasi, L. infantum e L. donovani anticorpos |
| Amostra | Sangue total, plasma ou soro canino |
| Tempo de leitura | 10 minutos |
| Quantidade | 1 caixa (kit) = 10 dispositivos (embalagem individual) |
| Conteúdo | Kit de teste, frasco tampão e conta-gotas descartável |
| Armazenar | Temperatura ambiente (de 2 a 30℃) |
| Vencimento | 24 meses após a fabricação |
| Cuidado | Use dentro de 10 minutos após a aberturaUse uma quantidade apropriada de amostra (0,01 ml de um conta-gotas) Use após 15 a 30 minutos em temperatura ambiente se forem armazenados em condições frias Considere os resultados do teste como inválidos após 10 minutos |
Informação
Os vermes cardíacos adultos crescem vários centímetros de comprimento e residem nas artérias pulmonares, onde podem obter nutrientes suficientes. Os vermes cardíacos dentro das artérias desencadeiam inflamação e formam hematomas. O coração, então, precisa bombear com mais frequência do que antes, à medida que os vermes cardíacos aumentam em número, bloqueando as artérias.
Quando a infecção piora (existem mais de 25 dirofilariose em um cão de 18 kg), os dirofilariose se movem para o átrio direito, bloqueando o fluxo sanguíneo.
Quando o número de dirofilariose atinge mais de 50, eles podem ocupar
átrios e ventrículos.
Quando infectado com mais de 100 dirofilarioses na parte direita do coração, o cão perde a função cardíaca e acaba morrendo. Esta doença fatal
fenômeno é chamado de “Síndrome de Caval”.
Ao contrário de outros parasitas, os vermes cardíacos depositam pequenos insetos chamados microfilárias. As microfilárias do mosquito se espalham para o cão quando o mosquito suga o sangue do animal. Os vermes cardíacos que conseguem sobreviver no hospedeiro por 2 anos morrem se não se transferirem para outro hospedeiro dentro desse período. Os parasitas que residem em uma cadela prenhe podem infectar seu embrião.
O exame precoce da dirofilariose é muito importante para eliminá-la. A dirofilariose passa por várias etapas, como L1, L2 e L3, incluindo a fase de transmissão por mosquito, até se tornar dirofilariose adulta.
Dirofilariose em mosquito
A microfilária no mosquito se desenvolve e se transforma em parasitas L2 e L3, capazes de infectar cães em poucas semanas. O crescimento depende do clima. A temperatura favorável para o parasita é acima de 13,9°C.
Quando um mosquito infectado pica um cão, a microfilária L3 penetra na pele. Na pele, a microfilária se desenvolve e se transforma em L4 por 1 a 2 semanas. Após permanecer na pele por 3 meses, a L4 se transforma em L5, que se espalha para o sangue.
L5, como forma adulta do verme do coração, entra no coração e nas artérias pulmonares, onde 5 a 7 meses depois os vermes do coração depositam os insetos.


Diagnóstico
O histórico da doença e os dados clínicos de um cão doente, além de vários métodos de diagnóstico, devem ser considerados no diagnóstico. Por exemplo, raio-X, ultrassonografia, exame de sangue, detecção de microfilárias e, no pior dos casos, autópsia são necessários.
Exame sérico;
Detecção de anticorpos ou antígenos no sangue
Exame de antígeno;
O objetivo é detectar antígenos específicos de dirofilariose adulta fêmea. O exame é realizado em ambiente hospitalar e sua taxa de sucesso é alta. Os kits de teste disponíveis no mercado são projetados para detectar dirofilariose adulta de 7 a 8 meses de idade, dificultando a detecção de dirofilariose com menos de 5 meses.
Tratamento
A infecção por dirofilariose é curada com sucesso na maioria dos casos. Para eliminar todos os tipos de dirofilariose, o uso de medicamentos é a melhor maneira. A detecção precoce da dirofilariose aumenta a taxa de sucesso do tratamento. No entanto, na fase avançada da infecção, podem ocorrer complicações, tornando o tratamento mais difícil.
Informação
A bactéria Anaplasma phagocytophilum (anteriormente Ehrilichia phagocytophila) pode causar infecção em várias espécies animais, incluindo humanos. A doença em ruminantes domésticos também é chamada de febre transmitida por carrapatos (TBF) e é conhecida há pelo menos 200 anos. Bactérias da família Anaplasmataceae são organismos gram-negativos, imóveis, cocoides a elipsoides, variando em tamanho de 0,2 a 2,0 µm de diâmetro. São aeróbios obrigatórios, sem uma via glicolítica, e todos são parasitas intracelulares obrigatórios. Todas as espécies do gênero Anaplasma habitam vacúolos revestidos por membrana em células hematopoiéticas imaturas ou maduras de hospedeiros mamíferos. Um phagocytophilum infecta neutrófilos e o termo granulocitotrópico refere-se a neutrófilos infectados. Raramente organismos foram encontrados em eosinófilos.
Anaplasma phagocytophilum
Sintomas
Sinais clínicos comuns deA anaplasmose canina inclui febre alta, letargia, depressão e poliartrite. Sinais neurológicos (ataxia, convulsões e dor no pescoço) também podem ser observados. A infecção por Anaplasma phagocytophilum raramente é fatal, a menos que seja complicada por outras infecções. Perdas diretas, condições incapacitantes e perdas de produção foram observadas em cordeiros. Aborto e espermatogênese prejudicada em ovinos e bovinos foram registrados. A gravidade da infecção é influenciada por vários fatores, como variantes de Anaplasma phagocytophilum envolvidas, outros patógenos, idade, estado imunológico e condição do hospedeiro, e fatores como clima e manejo. Deve-se mencionar que as manifestações clínicas em humanos variam de uma doença leve, autolimitada, semelhante à gripe, a uma infecção com risco de vida. No entanto, a maioria das infecções humanas provavelmente resulta em manifestações clínicas mínimas ou nenhuma.
Transmissão
Anaplasma phagocytophilum é transmitido por carrapatos ixodídeos. Nos Estados Unidos, os principais vetores são Ixodes scapularis e Ixodes pacificus, enquanto Ixode ricinus foi considerado o principal vetor exofílico na Europa. Anaplasma phagocytophilum é transmitido transestadialmente por esses carrapatos vetores, e não há evidências de transmissão transovariana. A maioria dos estudos até o momento que investigaram a importância dos hospedeiros mamíferos de A. phagocytophilum e seus carrapatos vetores se concentrou em roedores, mas este organismo possui uma ampla gama de hospedeiros mamíferos, infectando gatos, cães, ovelhas, vacas e cavalos domesticados.

Diagnóstico
A imunofluorescência indireta é o principal teste utilizado para detectar infecções. As amostras de soro nas fases aguda e convalescente podem ser avaliadas para detectar uma alteração de quatro vezes no título de anticorpos contra Anaplasma phagocytophilum. Inclusões intracelulares (móruleias) são visualizadas em granulócitos em esfregaços de sangue corados por Wright ou Gimsa. Métodos de reação em cadeia da polimerase (PCR) são utilizados para detectar DNA de Anaplasma phagocytophilum.
Prevenção
Não há vacina disponível para prevenir a infecção por Anaplasma phagocytophilum. A prevenção consiste em evitar a exposição ao carrapato vetor (Ixodes scapularis, Ixodes pacificus e Ixode ricinus) da primavera ao outono, usar profiláticamente antiacaricidas e usar profiláticamente doxiciclina ou tetraciclina ao visitar regiões endêmicas de carrapatos Ixodes scapularis, Ixodes pacificus e Ixode ricinus.
Informação
Ehrlichia canis é um parasita pequeno e em forma de bastonete, transmitido pelo carrapato marrom do cão, Rhipicephalus sanguineus. E. canis é a causa da ehrlichiose clássica em cães. Os cães podem ser infectados por diversas espécies de Ehrlichia, mas a mais comum causadora de ehrlichiose canina é a E. canis.
Sabe-se agora que o E. canis se espalhou por todos os Estados Unidos, Europa, América do Sul, Ásia e Mediterrâneo.
Cães infectados que não são tratados podem se tornar portadores assintomáticos da doença por anos e eventualmente morrer de hemorragia maciça.

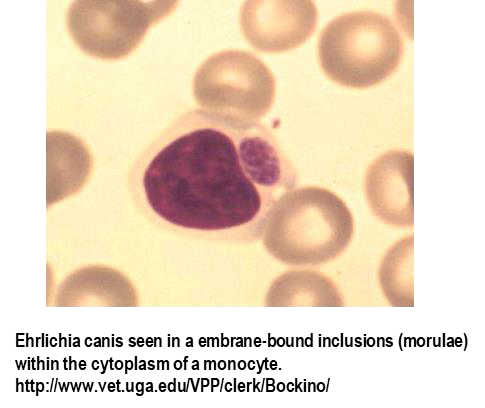
Sintomas
A infecção por Ehrlichia canis em cães é dividida em 3 estágios;
FASE AGUDA: Esta é geralmente uma fase muito branda. O cão estará apático, sem comida e pode apresentar linfonodos aumentados. Pode haver febre, mas raramente esta fase mata um cão. A maioria elimina o organismo por conta própria, mas alguns passam para a fase seguinte.
FASE SUBCLÍNICA: Nesta fase, o cão parece normal. O organismo está sequestrado no baço e, essencialmente, escondido lá.
FASE CRÔNICA: Nesta fase, o cão adoece novamente. Até 60% dos cães infectados com E. canis apresentam sangramento anormal devido à redução do número de plaquetas. Pode ocorrer inflamação profunda nos olhos, chamada "uveíte", como resultado da estimulação imunológica prolongada. Efeitos neurológicos também podem ser observados.
Diagnóstico e tratamento
O diagnóstico definitivo de Ehrlichia canis requer a visualização da mórula dentro de monócitos na citologia, detecção de anticorpos séricos de E. canis com o teste de imunofluorescência indireta (IFI), amplificação por reação em cadeia da polimerase (PCR) e/ou gel blotting (Western immunoblotting).
A base da prevenção da ehrlichiose canina é o controle de carrapatos. O medicamento de escolha para o tratamento de todas as formas de ehrlichiose é a doxiciclina por pelo menos um mês. Deve haver melhora clínica drástica dentro de 24 a 48 horas após o início do tratamento em cães com doença em fase aguda ou crônica leve. Durante esse período, a contagem de plaquetas começa a aumentar e deve retornar ao normal em até 14 dias após o início do tratamento.
Após a infecção, é possível ser reinfectado; a imunidade não dura após uma infecção anterior.
Prevenção
A melhor prevenção da ehrlichiose é manter os cães livres de carrapatos. Isso deve incluir a verificação diária da pele em busca de carrapatos e o tratamento dos cães com métodos de controle de carrapatos. Como os carrapatos transmitem outras doenças devastadoras, como a doença de Lyme, anaplasmose e febre maculosa das Montanhas Rochosas, é importante manter os cães livres de carrapatos.
Informação
A leishmaniose é uma doença parasitária grave e grave que afeta humanos, cães e felinos. O agente causador da leishmaniose é um protozoário pertencente ao complexo Leishmania donovani. Este parasita é amplamente distribuído em países temperados e subtropicais do sul da Europa, África, Ásia, América do Sul e América Central. Leishmania donovani infantum (L. infantum) é responsável pela doença felina e canina no sul da Europa, África e Ásia. A leishmaniose canina é uma doença sistêmica progressiva grave. Nem todos os cães desenvolvem a doença clínica após a inoculação com os parasitas. O desenvolvimento da doença clínica depende do tipo de resposta imune que cada animal apresenta.
contra os parasitas.
Sintomas
Em Canino
Manifestações viscerais e cutâneas podem ser encontradas simultaneamente em cães; diferentemente dos humanos, síndromes cutâneas e viscerais separadas não são observadas. Os sinais clínicos são variáveis e podem mimetizar outras infecções. Infecções assintomáticas também podem ocorrer. Os sinais viscerais típicos podem incluir febre (que pode ser intermitente), anemia, linfadenopatia, esplenomegalia, letargia, diminuição da tolerância ao exercício, perda de peso e diminuição do apetite. Sinais viscerais menos comuns incluem diarreia, vômitos, melena, glomerulonefrite, insuficiência hepática, epistaxe, poliúria-polidipsia, espirros, claudicação (devido a poliartrite ou miosite), ascite e colite crônica.
Em Felino
Gatos raramente são infectados. Na maioria dos gatos infectados, as lesões limitam-se a úlceras cutâneas crostosas, geralmente encontradas nos lábios, nariz, pálpebras ou pavilhão auricular. Lesões e sinais viscerais são raros.
Vida útil
O ciclo de vida se completa em dois hospedeiros: um hospedeiro vertebrado e um hospedeiro invertebrado (flebotomíneo). A fêmea do flebotomíneo se alimenta do hospedeiro vertebrado eIngere amastigotas. Promastigotas flageladas se desenvolvem no inseto. As promastigotas são injetadas no hospedeiro vertebrado durante a alimentação do flebotomíneo. As promastigotas se desenvolvem em amastigotas e se multiplicam principalmente nos macrófagos. A multiplicação dentro dos macrófagos da pele, mucosa e vísceras causa leishmaniose cutânea, mucosa e visceral, respectivamente.
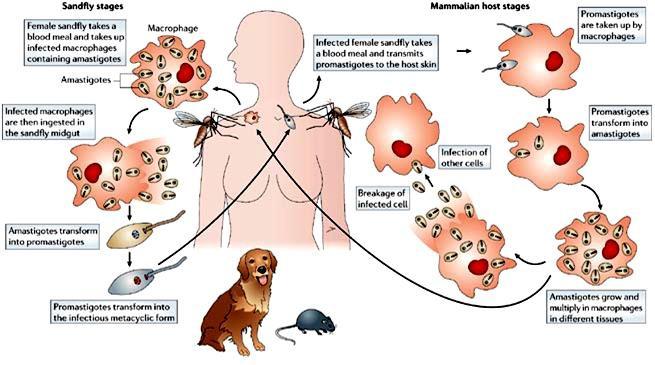
Diagnóstico
Em cães, a leishmaniose é geralmente diagnosticada pela observação direta dos parasitas, utilizando Giemsa ou colorações rápidas patenteadas, em esfregaços de aspirados de linfonodos, baço ou medula óssea, biópsias de tecido ou raspados de pele de lesões. Organismos também podem ser encontrados em lesões oculares, particularmente em granulomas. Os amastigotas são parasitas redondos a ovais, com um núcleo basofílico arredondado e um pequeno cinetoplasto em forma de bastonete. São encontrados em macrófagos ou liberados de células rompidas. Técnicas de imuno-histoquímica e reação em cadeia da polimerase (PCR) também são utilizadas.
Prevenção
Os medicamentos mais comumente utilizados são: Antimoniato de Meglumina associado a Alopurinol, Aminosidina e, recentemente, Anfotericina B. Todos esses medicamentos requerem um regime de doses múltiplas, o que dependerá da condição do paciente e da cooperação do tutor. Sugere-se que o tratamento de manutenção seja mantido com alopurinol, pois não é possível garantir que os cães não apresentarão recaídas se o tratamento for interrompido. O uso de coleiras contendo inseticidas, xampus ou sprays eficazes para proteger os cães contra picadas de flebotomíneos deve ser contínuo para todos os pacientes em tratamento. O controle do vetor é um dos aspectos mais importantes do controle da doença.
O mosquito-palha é vulnerável aos mesmos inseticidas que o vetor da malária.